HPV – PHÂN LOẠI VÀ SINH BỆNH HỌC
1. Phân loại các týp HPV
Trong hơn 200 týp HPV (Human Papillomavirus) đã được xác định, một số có thể lây truyền qua đường quan hệ tình dục (âm đạo, hậu môn, hoặc miệng). Các týp này thường được phân loại thành hai nhóm chính: nguy cơ thấp và nguy cơ cao1. Các týp nguy cơ thấp hiếm khi gây ung thư, trong khi các týp nguy cơ cao có khả năng dẫn đến các tổn thương tiền ung thư và ung thư.
Tuy nhiên, để phản ánh chính xác hơn về khả năng gây ung thư của từng týp, Cơ quan Nghiên cứu Ung thư Quốc tế (IARC) của Tổ chức Y tế Thế giới (WHO) đã cập nhật và đề xuất một cách phân loại mới. Cách phân loại này tập trung vào nhóm HPV nguy cơ cao, nay được gọi là “nhóm HPV sinh ung thư” gồm 12 týp2. Dựa trên tỉ lệ phần trăm nguy cơ quy trách ung thư cổ tử cung, IARC phân chia 12 týp này thành 4 nhóm nhỏ, trong đó HPV týp 16 và 18 là nguyên nhân của hầu hết các ca ung thư liên quan đến HPV (Bảng 1).
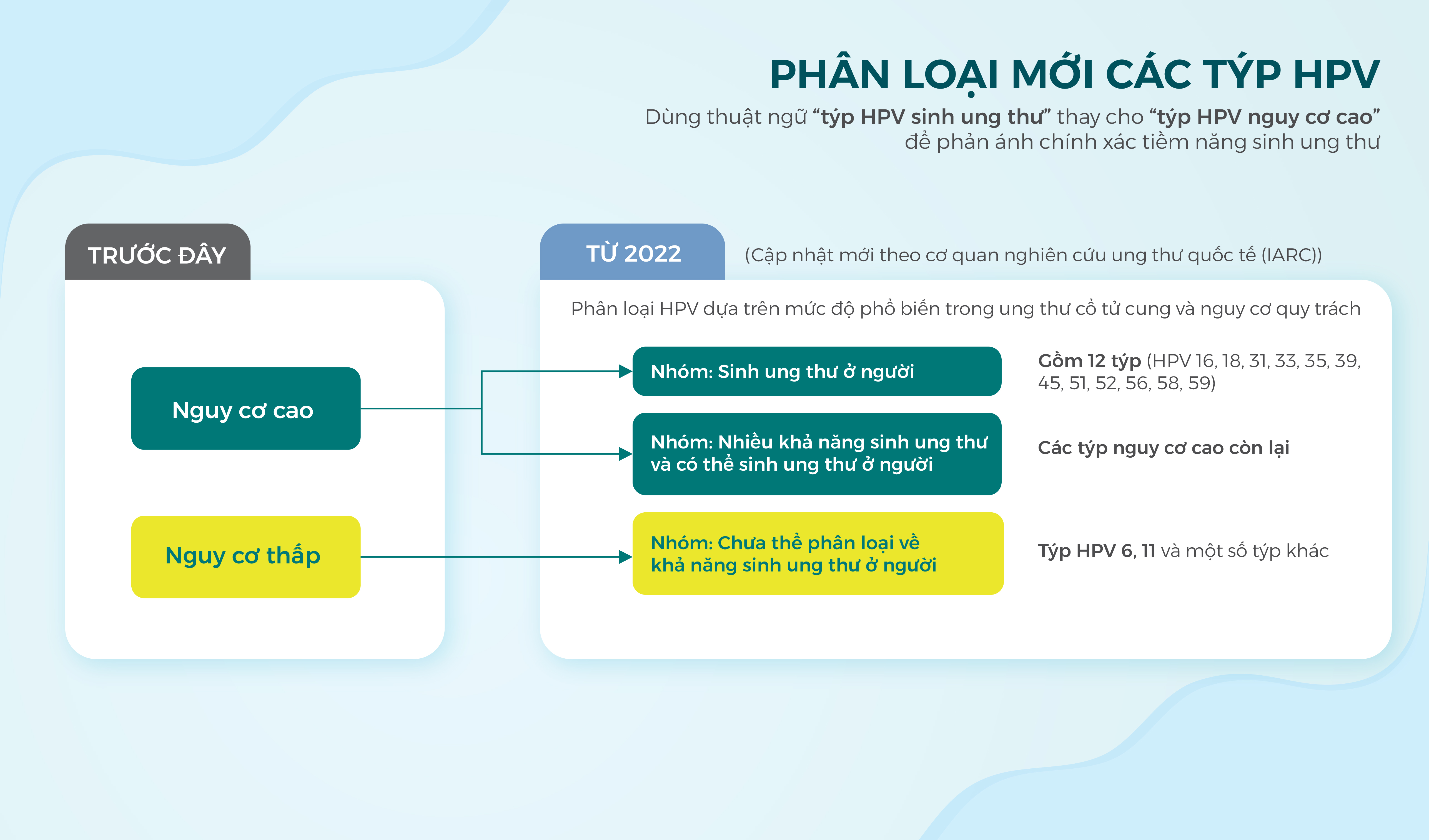
Bảng 1. Phân loại các týp HPV sinh ung thư2
| Nhóma | Týp HPV | Tỉ lệ lưu hành týp HPV ở những người mắc ung thư cổ tử cung xâm lấn (%) | Tỉ lệ lưu hành týp HPV ở những nguời có tế bào cổ tử cung bình thường (%) | Tỉ lệ nguy cơ quy trách (%)b |
| 1 | HPV16 | 55,8 | 2,6 | 62,4 |
| 2 | HPV18 | 14,3 | 1,0 | 15,3 |
| HPV45 | 4,8 | 0,6 | 4,8 | |
| 3 | HPV33 | 4,0 | 0,6 | 3,9 |
| HPV58 | 4,0 | 0,8 | 3,7 | |
| HPV31 | 3,5 | 1,0 | 2,9 | |
| HPV52 | 3,2 | 1,0 | 2,6 | |
| HPV35 | 1,6 | 0,4 | 1,4 | |
| 4 | HPV59 | 1,2 | 0,4 | 0,9 |
| HPV39 | 1,3 | 0,6 | 0,8 | |
| HPV51 | 1,0 | 0,9 | 0,2 | |
| HPV56 | 0,8 | 0,6 | 0,2 |
aPhân loại dựa trên tỉ lệ lưu hành của týp HPV ở những người mắc ung thư cổ tử cung.
bTỉ lệ nguy cơ quy trách là phần trăm ung thư cổ tử cung gây ra bởi týp HPV đó.
2. Sinh bệnh học
2.1 Vòng đời của HPV
Vi rút HPV xâm nhập vào tế bào vật chủ qua các vết thương hoặc tổn thương vi mô trên lớp biểu mô, từ đó lây nhiễm vào các tế bào biểu mô màng đáy3,4. Ở giai đoạn đầu của quá trình lây nhiễm, hệ gen DNA vòng sợi đôi của HPV ở trạng thái đóng vòng (episome) trong tế bào đáy với số lượng bản sao thấp3,4,5. Vi rút bắt đầu nhân lên nhờ sự hỗ trợ của các protein E1 và E23,4. Các tế bào bị nhiễm có thể ở màng đáy trong một thời gian dài4.
Khi các tế bào bị nhiễm di chuyển lên các lớp biểu mô phía trên, biểu hiện gen của vi rút trở nên mạnh mẽ4. Các protein sớm như E5, E6 và E7 tạo môi trường thuận lợi cho quá trình nhân lên của vi rút, bao gồm cả việc kích thích sự tăng sinh tế bào, ức chế quá trình chết theo chu trình (appotosis) của vật chủ và trốn tránh hệ miễn dịch vật chủ3,4. Khi các tế bào này hoàn thành quá trình biệt hoá ở các lớp trên của biểu mô, các gen L1 và L2 được biểu hiện và có liên quan đến quá trình tổng hợp capsid, lắp ráp thành virion hoàn chỉnh3,4. Các virion HPV được nhân lên ở lớp bề mặt của biểu mô và sau đó được giải phóng khỏi tế bào và bắt đầu đợt lây nhiễm mới4.
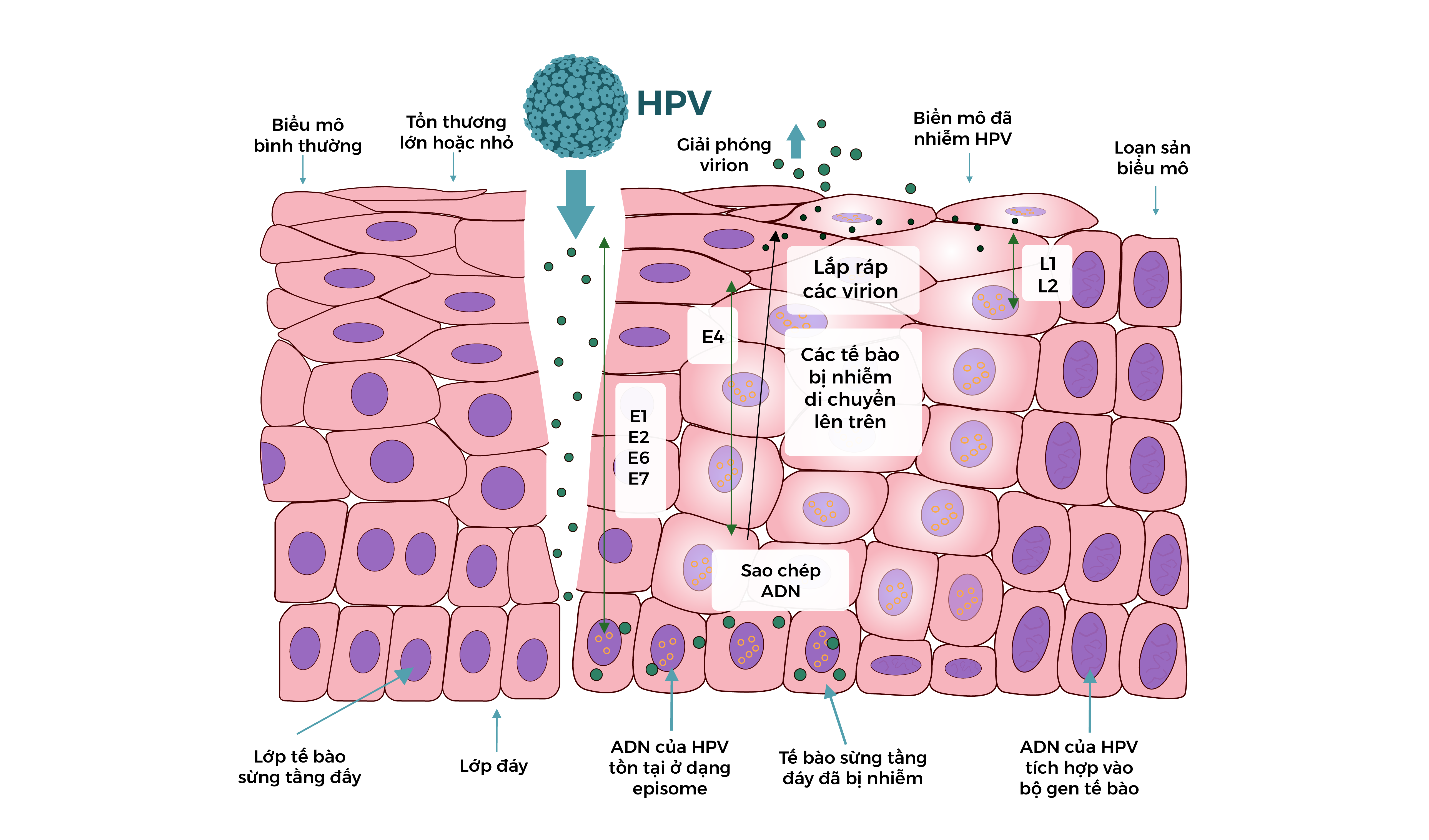
Hình 2. Vòng đời của HPV.
Các mũi tên xanh dương biểu hiện các gen sớm E1, E2, E4, E6, E7 và các gen muộn L1, L2 của HPV. (Điều chỉnh từ Mlynarczyk-Bonikowska B, Rudnicka L3)
2.2 Đáp ứng miễn dịch và sự lẩn tránh miễn dịch khi nhiễm HPV
Hệ miễn dịch vật chủ có vai trò quan trọng trong việc kiểm soát và đào thải vi rút HPV3,4. Phần lớn các trường hợp nhiễm HPV sẽ được hệ miễn dịch loại bỏ trước khi tiến triển thành ung thư4. Tuy nhiên, vi rút HPV đã phát triển các phương thức để lẩn tránh sự tiêu diệt của cả miễn dịch bẩm sinh và miễn dịch thích ứng4.
Một cơ chế chính mà HPV sử dụng để lẩn tránh hệ miễn dịch là tránh trình diện kháng nguyên4. Các protein E6 và E7 ức chế con đường truyền tín hiệu interferon, do đó làm giảm số lượng phân tử phức hợp tương hợp mô chính (MHC) lớp 1 trên bề mặt các tế bào trình diện kháng nguyên (APC) đang bị nhiễm HPV4. Các tế bào T gây độc tế bào CD8+ đóng vai trò quan trọng trong việc loại bỏ các tế bào bị nhiễm vi rút thông qua MHC lớp 14. Tuy nhiên, MHC lớp I không được biểu hiện trên bề mặt tế bào APC, dẫn đến việc không kích hoạt các tế bào T CD8+4. Sự lẩn tránh miễn dịch liên tục của vi rút dẫn đến sự tồn tại dai dẳng của vi rút và lâu dài là sự hình thành ung thư4.
2.3 Cơ chế gây tổn thương tiền ung thư và tân sinh khi nhiễm HPV
Các protein sớm của vi rút HPV như E5, E6 và E7 đóng vai trò quan trọng nhất trong quá trình bệnh sinh của các tổn thương tân sinh (ung thư) phát sinh do nhiễm HPV3.
Protein E5 có trong tất cả các týp HPV có nguy cơ cao gây ung thư lây nhiễm qua niêm mạc, hoạt động như một protein ung thư giai đoạn sớm3. Protein E5 chịu trách nhiệm kiểm soát sự phát triển của tế bào, quá trình biệt hóa và điều hòa miễn dịch3. Nó được biểu hiện trong giai đoạn đầu của quá trình sao chép3. Các protein E5 nhỏ, kỵ nước, đơn lẻ được hình thành, sau đó khuếch tán qua màng, liên kết với các thụ thể yếu tố tăng trưởng có nguồn gốc từ tiểu cầu và biểu bì (PDGFR, EGFR), tăng cường tín hiệu của các thụ thể này, dẫn đến ức chế quá trình chết theo chu trình và kích thích quá trình tăng sinh3.
Protein E6 là một protein ung thư chính trong sự phát triển ung thư liên quan đến HPV3,4. Cơ chế quan trọng của E6 là liên kết và bất hoạt protein ức chế khối u p533,4. Việc này dẫn đến sự phân hủy p533,4, làm cho tế bào mất đi khả năng kiểm soát chu kỳ phân chia, góp phần gây mất ổn định bộ gen và tích lũy đột biến4,5. E6 cũng ngăn chặn quá trình chết theo chu trình và góp phần làm bất tử hóa tế bào3,4.
Các protein sớm của vi rút HPV như E5, E6 và E7 đóng vai trò quan trọng nhất trong quá trình bệnh sinh của các tổn thương tân sinh (ung thư) phát sinh do nhiễm HPV3.
Protein E5 có trong tất cả các týp HPV có nguy cơ cao gây ung thư lây nhiễm qua niêm mạc, hoạt động như một protein ung thư giai đoạn sớm3. Protein E5 chịu trách nhiệm kiểm soát sự phát triển của tế bào, quá trình biệt hóa và điều hòa miễn dịch3. Nó được biểu hiện trong giai đoạn đầu của quá trình sao chép3. Các protein E5 nhỏ, kỵ nước, đơn lẻ được hình thành, sau đó khuếch tán qua màng, liên kết với các thụ thể yếu tố tăng trưởng có nguồn gốc từ tiểu cầu và biểu bì (PDGFR, EGFR), tăng cường tín hiệu của các thụ thể này, dẫn đến ức chế quá trình chết theo chu trình và kích thích quá trình tăng sinh3.
Protein E6 là một protein ung thư chính trong sự phát triển ung thư liên quan đến HPV3,4. Cơ chế quan trọng của E6 là liên kết và bất hoạt protein ức chế khối u p533,4. Việc này dẫn đến sự phân hủy p533,4, làm cho tế bào mất đi khả năng kiểm soát chu kỳ phân chia, góp phần gây mất ổn định bộ gen và tích lũy đột biến4,5. E6 cũng ngăn chặn quá trình chết theo chu trình và góp phần làm bất tử hóa tế bào3,4.
Protein E7 cũng là một protein sinh ung thư quan trọng3,4. Chức năng chính của E7 là nhắm mục tiêu và làm bất hoạt protein ức chế khối u Rb3,4. Sự bất hoạt Rb dẫn đến việc giải phóng các yếu tố thúc đẩy chu kỳ tế bào (như E2F), khiến tế bào tăng sinh không kiểm soát3,4. Sự tương tác của E6 với p53 và E7 với Rb làm tăng khả năng bất tử hóa và mất ổn định bộ gen, thúc đẩy sự phát triển của các tế bào đột biến thành tổn thương tiền ung thư và ung thư3,4.
Những ý chính
⦁ HPV được phân loại theo nguy cơ sinh ung thư thành hai nhóm: nguy cơ cao và nguy cơ thấp1. Trong nhóm nguy cơ cao, IARC xác định 12 týp “sinh ung thư” và phân chúng thành 4 nhóm nhỏ dựa trên tỉ lệ nguy cơ quy trách đối với ung thư cổ tử cung1.
⦁ Vòng đời HPV bắt đầu khi vi rút xâm nhập qua tổn thương vi mô, tồn tại ở lớp tế bào đáy, nhân lên và tạo virion ở lớp biểu mô trên3,4.
⦁ HPV phát triển khả năng trốn tránh miễn dịch nhờ protein E6 và E7, cho phép vi rút tồn tại dai dẳng, và lâu dài có thể dẫn đến ung thư4.
⦁ Trong quá trình ung thư hóa do nhiễm HPV, protein E5, E6, E7 đóng vai trò quan trọng3.
Chú thích
IARC = International Agency for Research on Cancer = Cơ quan Nghiên cứu Ung thư Quốc tế;
WHO = World Health Organization = Tổ chức Y tế Thế giới
ADN = Acid deoxyribonucleic;
MHC lớp 1 = Major Histocompatibility Complex Class I = Phức hợp tương hợp mô chính lớp 1;
APC = Antigen presenting cells = Tế bào trình diện kháng nguyên;
CD8 = Cluster of Differentiation 8 = Cụm biệt hoá 8;
PDGFR = Platelet-derived growth factor receptor = Thụ thể yếu tố tăng trưởng có nguồn gốc từ tiểu huyết cầu;
EGFR = Epidermal growth factor receptor = Thụ thể yếu tố tăng trưởng biểu bì;
Tài liệu tham khảo
1. NIH. National Cancer Institute. HPV and Cancer. https://www.cancer.gov/about-cancer/causes-prevention/risk/infectious-agents/hpv-and-cancer. Accessed 31 May 2025.
2. IARC 2024. Target product profiles for human papillomavirus screening tests to detect cervical pre-cancer and cancer. Available at: https://iris.who.int/bitstream/handle/10665/379099/9789240100275-eng.pdf. Accessed 31 May 2025.
3. Mlynarczyk-Bonikowska, B., & Rudnicka, L. (2024). HPV Infections-Classification, Pathogenesis, and Potential New Therapies. International journal of molecular sciences, 25(14), 7616. https://doi.org/10.3390/ijms25147616.
4. Senba, M., & Mori, N. (2012). Mechanisms of virus immune evasion lead to development from chronic inflammation to cancer formation associated with human papillomavirus infection. Oncology reviews, 6(2), e17. https://doi.org/10.4081/oncol.2012.e17.
5. Hội Y Học Dự Phòng Việt Nam (2018). Chẩn đoán, điều trị và dự phòng nhiễm HPV và ung thư cổ tử cung. Hà Nội: Nhà xuất bản Y học.
BÀI VIẾT CÙNG CHỦ ĐỀ


Tình hình nhiễm HPV và các bệnh có liên quan
HPV là một trong những bệnh lây truyền qua đường tình dục phổ biến nhất trên toàn cầu.
HPV – Vi rút gây u nhú ở người
Tìm hiểu về tỷ lệ nhiễm HPV trên toàn cầu, theo khu vực, giới tính, tuổi, týp vi rút và số ca mắc mới ung thư do HPV.

Phương thức lây truyền HPV
Tìm hiểu về HPV, vi rút có thể lây qua cả đường tình dục và ngoài quan hệ tình dục, với nguy cơ khác nhau tùy giới tính, hành vi
THƯ VIỆN KHOA HỌC VÀ THỰC HÀNH

Hiểu về HPV
Tìm hiểu bức tranh tổng quan về HPV, từ đặc điểm sinh bệnh học, phương thức lây truyền đến dữ liệu dịch tễ trong cộng đồng

Ung thư và bệnh lý liên quan đến HPV
Tìm hiểu ung thư và các bệnh lý liên quan đến HPV, từ biểu hiện lâm sàng đến dự phòng và điều trị

Vắc xin HPV
Tìm hiểu về vắc xin HPV và những tài liệu chuyên môn hướng dẫn dự phòng và kiểm soát các bệnh lý, ung thư liên quan HPV
VN-GSL-03075 17092027
